Vielleicht haben sie heute die ihnen bisher unbekante Diagnose POTS bekommen und möchten sich über diese „Krankheit“ informieren? Dann sind sie hier auf jeden Fall richtig. Weiterlesen
Was PoTSies vor dem Kauf ihrer Kompressionskleidung wissen sollten!
Vorneweg ein großes Dankeschon an Andrea, die sich sehr mit dem Kauf von für sie geeigneter Kompression auseinandersetzen musste und die ihre Erfahrungen hier mit uns teilt:
Theorie
Es gibt 2 verschiedene Arten von Gestricken:
1) Rundstrick
Wird hauptsächlich bei PoTS und bei Venenerkrankungen eingesetzt. Rundstrick ist wesentlich dünner als Flachstrick.
2) Flachstrick
Wird für Lipödem/ Lymphödem eingesetzt
Kann auch bei PoTS mit besonderer Begründung vom Arzt eingesetzt werden, und zwar wenn Rundstrick nicht funktioniert (z. B. wenn der Umfang der Oberschenkel sehr von dem der Knöchel abweicht, denn dann können bei Rundstrick bei der Herstellung nicht genügend Maschen zugefügt werden. Dies ist auch möglich, wenn kein Lipödem vorliegt).
Flachstrick wird von der Maschine für die Beine in einem Stück hergestellt und hinten zusammengenäht.
Auch Menschen mit Ehlers-Danlos-Syndrom tragen oft Flachstrick
Serie oder Maßanfertigung
Es gibt bei Rundstrick Serie oder Maßanfertigung.
Serienstrumpfware ist so hergestellt, dass sie für verschiedene Menschen passen würde und ist daher etwas günstiger.
Auch wenn es unlogisch erscheint: wenn es Probleme mit der Passform bei der Maßanfertigung gibt, lohnt es sich die Serie auszuprobieren. Oftmals sitzt sie besser, besonders am Knie.
Die Verordnung
Was muss auf dem Rezept stehen?
- Eine Kompressionsstrumpfhose ( oder Kompression AT) oder ein Paar Oberschenkelstrümpfe (oder Kompression AG)
- Rundstrick oder Flachstrick – Wenn nichts auf dem Rezept steht, wird Rundstrick angefertigt
- die Kompressionsklasse ( CCL), gibt es ab 1, bei PoTS wird meistens 2 angewendet, bei Bedarf auch 3
- nach Maß
- die Diagnose
Fakultativ
- offene oder geschlossene Fußspitze, bei Oberschenkelstrümpfen mit Haftrand
- bei Flachstrick ist auch eine Leggings möglich (Kompression BT)
Was kann noch auf dem Rezept stehen? Was sollte dazu bedacht werden?
Bei der 1. Verordnung ist es möglich, sich zwei Rezepte ausstellen zu lassen, auf dem 2. steht dann das gleiche wie auf dem erstem und zusätzlich „Wechselpaar aus hygienischen Gründen“
Bei Folgerezepten ist es sinnvoll, dass auch darauf steht: „Ersatzbeschaffung wegen Verschleiß“, auch wenn man die neue Versorgung so beantragt wie sie einem zusteht, da manche Krankenkassen in letzter Zeit ansonsten ablehnen, selbst wenn man erst später als 6 Monate beantragt.
Es stehen einem zwei Paar pro Jahr zu, und zwar nicht pro Kalenderjahr, sondern z. B. von Mai bis Mai.
Wenn man sich beim ersten Mal das Wechselpaar verschreiben lassen hat, hat man erst nach 1 Jahr Anspruch auf ein neues Paar.
Ansonsten alle 6 Monate.
Sollten die Strümpfe kaputtgehen, kann man mit dem Arzt wegen Verschleiß versuchen, über die Krankenkasse neue Strümpfe zu bekommen („wegen Verschleiß“ reicht als Begründung aus).
Die Krankenkasse kann aber ablehnen, deshalb als Absicherung kann man immer dazuschreiben lassen: „nach Kostenübernahme durch die Krankenkasse“. Ansonsten muss man selbst bezahlen, wenn die Krankenkasse die Kostenübernahme ablehnt.
Bei PoTS Patienten steht als Diagnose meistens auf dem Rezept CVI (chronisch venöse Insuffizienz), wenn es Rundstrick werden soll.
Ist Rundstrick nicht geeignet und es wird Flachstrick benötigt, so muss als Begründung vom Arzt entweder eine Diagnose Lip- oder Lymphödem vorliegen und auf dem Rezept notiert sein oder „Rundstrick ist nicht ausreichend“.
Beim Kauf
Einlösen kann man das Rezept in Sanitätshäusern oder in manchen Apotheken.
Die Sanitätshäuser und Apotheken haben meistens Verträge mit bestimmten Firmen.
Das heißt aber nicht, dass die Krankenkasse nur diese eine Firma bezahlt.
Manchmal versuchen Sanitätshäuser Aufschläge zu nehmen, wenn man eine bestimmte Firma oder Farbe wünscht.
Das ist aber nicht richtig. Notfalls vorher noch mal bei der Krankenkasse erkundigen.
Bei Farben gibt es Ausnahmen: für Trendfarben muss ein Aufschlag bezahlt werden.
Aufschläge dürfen sie nehmen, wenn man eine Zusatzausstattung wünscht wie z. B. Strasssteine oder spezielle Funktionen, die nicht notwendig sind, z. B. bei Flachstrick damit der Po hübscher aussieht.
Bei Flachstrick sind noch viele Extras möglich, die der Arzt auch verschreiben kann, z. B. Reißverschlüsse zur Erleichterung beim Anziehen oder auch Futterstoff für die Knieregion damit keine Einschnürungen entstehen (auf dem Rezept steht dann „Futterstoff bei CE“).
Bei beiden Materialarten sind auch Ausschnitte z. B. für die Stomaversorgung oder ein offener Schritt (wegen gyn. Pilzinfektionen oder Inkontinenz) möglich, aber das muss dann auch auf dem Rezept stehen
Pflege der Kompression
Um das Gestrick bei Rundstrick zu schützen, ist es empfehlenswert ein paar Dinge zu beachten:
- Nur mit Handschuhen anziehen (ich komme am besten mit Gummihandschuhen klar, andere mit Textilhandschuhen, die beschichtet sind).
- Auf die Länge der (Fuß) Nägel achten
- jeden Abend waschen macht das Gestrick wohl stabiler
- entweder per Hand waschen oder in der Waschmaschine (dann in einem Schutzbeutel/Netz, bei 20-30 Grad, Kurzprogramm)
- spezielles Waschmittel verwenden, nicht alle sind geeignet um Kompression zu erhalten
- trocknen im Liegen auf einem Handtuch vermeidet Laufmaschen durch kantigen Wäscheständer
- bestimmte Cremes dürfen nicht benutzt werden (siehe Information beim Kauf), da sie das Elasthan auflösen können (auch bei Physiotherapie darauf achten)
Sonstige Hinweise
Anziehhilfen: Wenn Gummihandschuhe zum Anziehen nicht ausreichen, kann der Arzt auch Anziehhilfen verordnen.
Es gibt eine Auswahl verschiedener Möglichkeiten von Gleitmaterialien bis zu Gestellen.
Am besten zuerst im Sanitätshaus beraten lassen und dann zum Arzt gehen.
Kompression mit offenen Spitzen lassen sich leichter anziehen, da man „Slippies“, eine Art Pantoffel, benutzen kann.
Es gibt sie aus beschichtetem Papier und aus einer Art Kunstseide.
Es ist wie bei den Handschuhen: jede/jeder muss selbst ausprobieren, womit es am besten geht.
Die Kompression sollte gleich morgens nach dem Waschen angezogen werden.
Am Anfang ist das sehr anstrengend. Nur Mut!
(Ich habe anfangs mit Hilfe 15 Minuten benötigt.)
Mit Übung ist es alleine in 2 Minuten zu schaffen
Bei Feuchtigkeit lässt sich die Kompression wesentlich schlechter anziehen, also entweder überlegen abends zu duschen oder kurz ablüften.
Zum Anziehen am besten wieder ins Bett legen.
Der beste Erfolg wird erreicht, wenn man die Kompression wirklich jeden Tag von morgens an trägt. Kniestrümpfe bringen nur wenigen PoTSies etwas, Strumpfhosen sind besser in der Wirkung als Strümpfe, sind jedoch teurer, schwieriger beim Anziehen und haben einen höheren Verschleiß. Evtl. kombinieren mit Miederwaren mit angeschnittenen Beinen (Kompression von Bauch und oberer Teil Oberschenkel).
Bauchkompression
Eine Bauchkompression oder Abdominal-Kompression kann extra verschrieben werden als Thorax-Abdominal-Stütze :
Es gibt 2 verschiedene Formen: Soft und mit Stäben an der Seite
Die Stäbe haben den Vorteil, dass sich die Bandage nicht einrollt, aber den Nachteil, dass sie in die Rippen pieken können.
Es gibt sie in unterschiedlichen Höhen, damit kann nur ein Stückchen komprimiert werden oder bis fast unter die Brust, auch ist die Rumpflänge von Mensch zu Mensch verschieden.
Es muss wieder ausprobiert werden, was vertragen wird.
Auf dem Rezept sollte neben Thorax-Abdominal-Stütze die Diagnose stehen (z. B. I 95.1, G90.8 und Bindegewebsschwäche).
Es ist auch möglich, die Bauchkompression in die Strumpfhosen einzuarbeiten. Dies gibt es auch bei Serien, aber nicht bei allen Firmen und Modellen.
Doch man ist unabhängiger, wenn man die Bauchkompression extra hat.
Zudem vertragen nicht alle POTSies eine Bauchkompression, z. B. bei Darmproblemen.
Armkompression
Evtl. ist auch eine Kompression an den Armen notwendig.
Wenn man an den Beinen eine Kompressionsklasse 2 benötigt, heißt das nicht, dass man automatisch auch an den Armen eine 2 braucht!
Hier besser erst mit CCL 1 anfangen.
Armkompression gibt es auch wieder in Rundstrick und Flachstrick, bei Flachstrick wieder mehr Möglichkeiten für individuelle Anpassungen.
Es gibt auch aus dem Sportbereich Kompressionen für die Arme, die sind zwar wesentlich günstiger, werden aber nicht von der Krankenkasse übernommen, da sie keine Hilfsmittelnummer haben.
Persönliche Erfahrungen – die Praxis
(von Andrea, jede/jeder kann das ganz anders empfinden)
1) Flachstrick ist leichter anzuziehen, weniger anfällig für Verschleiß, deutlich besser zu individualisieren, aber auch viel dicker vom Stoff, daher im Sommer für mich nicht machbar, außerdem sehr teuer (ca. ab 600,- ohne besondere Extras, jedoch mit Kniefutterstoff)
2) Rundstrick ist im Sommer angenehmer, günstiger in der Anschaffung (Maß ca. 150,- bis 200,-, Serie ab ca. 65,- im Angebot bis ca. 100,-), bekommt jedoch schnell Löcher und Laufmaschen.
Was angenehmer auf der Haut empfunden wird, ist individuell.
Bei Rundstrick fühlt sich auch jedes Modell auf der Haut anders an.
Es kann also länger dauern, bis man das optimale Modell für sich gefunden hat.
Insgesamt reichen zwei Paar Strümpfe meistens nicht im Jahr, selbst bei vorsorglichem Umgang. Die Haltbarkeit der Strümpfe ist abhängig vom Hersteller, dem Material, der Passform hängt.
Aber selbst bei guten und haltbaren Strümpfen, ist es empfehlenswert, Ersatz zu haben. Wenn man z. B. verreist oder ins Krankenhaus muss, ist es nicht immer möglich zu waschen, um jeden Tag frische Strümpfe anziehen zu können.
Bei Serienstrümpfen lohnt es sich, nach Angeboten zu suchen.
Bisher sind Serienstrümpfe für mich ein Kompromiss, der von der Kompression her funktioniert, aber nicht 100% passend ist für meine Bedürfnisse (offene Spitze, die nicht zu lang ist, Strumpfhose, die ein hohes Leibteil hat, ich reagiere oft auf Haftbänder mit Quaddeln)
Achtung: es ist nicht bei allen Firmen eine Rückgabe möglich
Trend und Sonderfarben sind immer von der Rückgabe ausgeschlossen!
Es ist übrigens nicht schwer selbst zu messen.
Es gibt bei jeder Firma Tabellen mit den Maßen.
Leider hat jede Firma ihre eigenen Tabellen, das heißt unübersichtlich am Anfang. Teilweise gibt es sogar für einzelne Modelle andere Tabellen, hat aber den Vorteil, dass wahrscheinlich jede irgendeine passende Versorgung finden wird.
A Fußumfang
Y Umfang bei gestrecktem Fuß Höhe Spann
B Fessel
B1 Wade zwischen Fessel und dickster Stelle der Wade
C dickste Stelle der Wade
D kurz unter Knie
E kurz über Knie
F Mitte zwischen E und G
G dickste Stelle Oberschenkel, da wo Strumpf aufhören würde ( 3 Finger breit unter dem Po)
H Hüfte
T Taille
Man braucht noch das Längenmaß bis G oder für Strumpfhose den Schritt, erfahrungsgemäß wenn man genau auf der Grenze zwischen 2 Längen liegt, lieber die Längere nehmen
Haben die Strümpfe oder die Strumpfhose ein Loch, kann man sie reparieren lassen. Das kann sich bei noch guten Strümpfen sehr rentieren – dazu natürlich das Loch, die Laufmasche nicht groß werden lassen.
persöhnliche Erfahrungen mit Strümpfen verschiedener Hersteller von Andrea H.:
“Ratgeber Ehlers-Danlos-Syndrome; Komplexe Bindegewebserkrankungen einfach erklärt”
Heiß erwartet und nun endlich da: der “Ratgeber Ehlers-Danlos-Syndrome; Komplexe Bindegewebserkrankungen einfach erklärt” von Karina Sturm, Frau Dr. Andrea Maier und Frau Dr. Helena Jung. Ich hatte beim diesjährigen Symposium von POTS und andere Dysautonomien e.V. schon einen kleinen Einblick in die wirklich wertvolle Informationssammlung dieses Buches bekommen und hier nun die Beschreibung von Karina selbst:
Liebe Mitstreiter*innen,
Ich freue mich Ihnen mitteilen zu dürfen, dass Sie seit dieser Woche den ersten Ratgeber zum Thema Ehlers-Danlos-Syndrome im Handel erwerben können. Unter dem Titel “Ratgeber Ehlers-Danlos-Syndrome; Komplexe Bindegewebserkrankungen einfach erklärt” erschien dieser im renommierten Springer Nature Verlag.
WeiterlesenEinleitung – Warum ist das Atmen ein wichtiges Thema?
Unser Atem ist der große Dirigent unseres Körpers. Er dirigiert unseren autonomen Tonus, unsere Gefühle und unsere Entscheidungsfindungsprozesse. Er ist das eine, auf das Menschen nicht länger als ein paar Minuten verzichten können, doch die meisten atmen ihr ganzes Leben lang, ohne darüber nachzudenken, das Atmen läuft völlig unbewusst ab. Doch der Atem kann ein Werkzeug werden, das wir nutzen können, um die Kontrolle über die Verbindung von Körper zu Gefühlswelt zu erlangen.
Bei Menschen mit Fehlfunktionen des Autonomen Nervensystems – allg. Dysautonomien, POTS, ME/CFS, Post-Covid-19 – ist der Atem häufig aus dem Takt gekommen, deshalb ist Atmen ein sehr wichtiges Thema, das bei der Therapie nicht außer acht gelassen werden darf.
Der Atem, ein wertvolles Werkzeug
Die Mechanik der Atmung, die Chemie und die Atemfrequenz sind wirkungsvoll und beeinflussen die mentale Gesundheit, die sportliche Leistung, das Verhalten bei Stress, die Meditation/Achtsamkeit und insgesamt die Gesundheit. Wir dürfen diese wichtige Komponente nicht vernachlässigen. Die Leistungsfähigkeit des Menschen sinkt, wenn der Stress zunimmt – ohne die richtigen Techniken und das richtige Bewusstsein für den Atem nimmt die Atemleistung ab. Weiterlesen
POTS und Dysautonomien – Von Kopf bis Fuß
Dieses Jahr wird es wieder ein Symposium mit den Themen POTS und Dysaitnomien geben. Und aufgrund von Corona wird es ONLINE stattfinden. Das heißt, jeder kann teilnehmen, solange er oder sie Zeit, einen online Zugang und das technische Gerät hat. Organisiert wird diese Veranstaltung vom Verein POTS und andere Dysautonomien. Sie richtet sich an alle POTS-Patienten, ihre Angehörige, behandelnde Ärzte und Interessierte. Das Thema des diesjährigen Symposiums ist POTS und andere Dysautonomien – Von Kopf bis Fuß.
WANN? Am Sonntag, den 31. Oktober 2021, ab 10:30
WO? per Zoom
Außerdem: steht der Film „Behind the Visible“
im Rahmen des Dysautonomiemonats für alle angemeldeten Teilnehmer kostenlos vom 22.-31. Oktober 2021 online zur Verfügung.
KOSTEN? Teilnahmegebühr: 10€ für Vereinsmitglieder kostenlos.
Weitere Informationen, Programm, Anmeldung?
linhttps://www.pots-dysautonomia.net/symposium2021
wir treffen uns!
Am Dienstag, 19.01.2021 wird im Rahmen der NDR Visite ab 20:15 Uhr das Diagnose-Abenteuer (wahrscheinlich ab 21:00) von Martina Hahn gezeigt. Martina hat das Ehlers-Danlos-Syndrom und in Folge leider auch ein POTS entwickelt. Schaltet rechtzeitig ein – Für zu spät gekommene oder zum wiederholten Ansehen gibt es ja zum Glück die Mediathek des NDR.
mediathek ndr abenteuer diagnose – Bing video


Ich wünschte, es gäbe für mich keinen Anlass einen Blogbeitrag zu POTS und LongCovid zu schreiben.
Letztes Frühjahr hatte ich mit Staunen und mit Schrecken beobachtet, wie in der Öffentlichkeit geglaubt wurde, die Epidemie in China würde uns in Deutschland nicht wirklich ernsthaft betreffen – ausgenommen natürlich Lieferschwierigkeiten aus China. Das Ansteckungsgeschehen bei Webasto war erkannt, unterbrochen und gemeistert worden. Wir haben alles im Griff, hat es geheißen. Mediziner haben uns erklärt, der neuartige Virus aus China, SARS CoV2 genannt, wäre nur wie eine Grippe – ja, auch Dr. Drosten hat diese Meinung bei seinem ersten öffentlichen Auftritt zum Thema vertreten. Nun es kam ganz anders….
WeiterlesenFast ohne Ausnahme berichten Patienten und Patientinnen mit POTS, dass sie nicht nur beim Stehen Symptome wie Brainfog („Nebel im Kopf“, Konzentrationsschwierigkeiten, Wortfindungsstörungen, o.ä.) haben sondern dass sie sich auch im Sitzen nur eine bestimmte Zeit gut konzentrieren können Symptome auch im Sitzen. Dass bei POTS die Versorgung des Gehirns beim Stehen schlechter ist, wurde schon durch mehrere Studien bestätigt. Doch was ist mit den Problemen bei der Konzentration im Sitzen?
Der Frage, welche Physiologie liegt dem „Brainfog“ in Abwesenheit von orthostatischem Stress bei POTS zugrunde, ist eine Forschergruppe des Departments of Cardiology, Centre for Heart Rhythm Disorders, des Royal Adelaide Hospitals in Adelaide, Australien, nachgegangen. Link zur Studie
Untersucht wurden die kognitiven und hämodynamischen Reaktionen (kardiovaskulär und zerebral: Herzfrequenz, Blutdruck, Kohlendioxid und zerebrale Blutflussgeschwindigkeit in der mittleren Hirnarterie) und zwar bei Studienbeginn, nach einem initialen kognitiven Test und anschließend nach einem (30-minütigen) verlängerten kognitiven Stresstest im Sitzen, sowie nach 5-minütigem Stehen.
Getestet wurden 22 Teilnehmer mit POTS und 18 gesunde aber ansonsten ähnliche Kontrollpersonen. Der Schweregrad der Symptome wurde mit einem Fragebogen zur orthostatischen Hypotonie zu Beginn und am Ende der Studie quantifiziert. Die zerebrale Blutflussgeschwindigkeit verringerte sich in beiden Gruppen nach dem verlängerten kognitiven Stresstest, aber in der POTS-Gruppe wurde eine stärkere Reduktion der zerebrale Blutflussgeschwindigkeit gegenüber der Kontrollgruppe beobachtet (-7,8% versus -1,8%). Bemerkenswerterweise war in der POTS-Gruppe die zerebrale Blutflussgeschwindigkeit nach dem verlängerten kognitiven Stresstest der POTS-Gruppe ähnlich reduziert wie die während der orthostatischen Belastung beobachteten Reduzierung (60,0±14,9 versus 60,4±14,8 cm/s). Darüber hinaus führte der verlängerte kognitive Stresstest bei den POTS-Patienten zu einer stärkeren Verlangsamung der psychomotorischen Geschwindigkeit (6,1 % versus 1,4 %) und zu einem stärkeren Anstieg der Symptomscores zum Ende der Tests, einschließlich erhöhter Konzentrationsschwierigkeiten. Alle anderen physiologischen Reaktionen (Blutdruck und endtidales Kohlendioxid) unterschieden sich zwischen den Gruppen nicht nach den verlängerten kognitiven Stresstest.
Schlussfolgerung:
Reduzierte zerebrale Blutflussgeschwindigkeit und kognitive Dysfunktion waren bei Patienten mit POTS nach längerer kognitiver Belastung auch ohne orthostatische Belastung evident.
2 Fragen zu psychosomatischen Diagnosen
MCAS oder das Mastzellaktivierungssyndrom ist eines der häufigen Ko-Erkrankungen zu POTS — sieht es nur für mich so aus, als ob man mit dem Posturalen (orthostatischem) Tachykardiesyndrom prädestiniert dafür ist, evtl. noch weitere Wortungetüme sammelt, ich sage nur: Myalgische Enzephalomyelits, Small Fiber (Poly) Neuropathie, hypermobiles Ehlers-Danlos-Syndrom, …
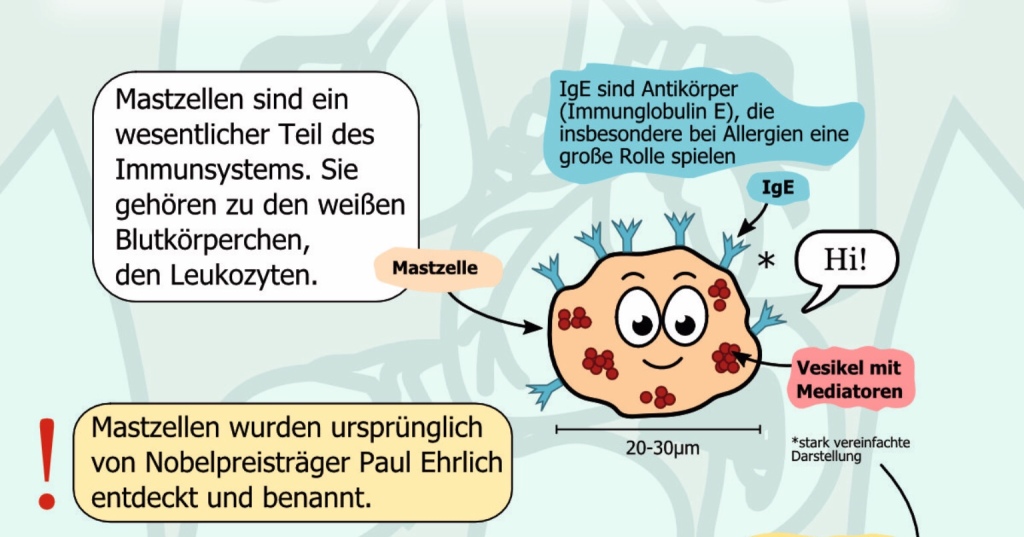
Egal, zum Glück gibt es Menschen wie Melanie Ludwig, die es nach intensiver Recherche und mit viel gestalterischem Können geschafft hat, dem Wortungetüm Mastzellaktivierungsstörung Leben einzuhauchen. Darf ich vorstellen:
(M)Ein Comic über das Mastzellaktivierungssyndrom ein med. Comic von Melanie Ludwig
In einer meiner Beiträgen findet sich ein Links zur Schwindelambulanz Sinsheim. Inzwischen wurde ich auf ein haarsträubendes Video zum Thema Coronavirus eines drt arbeitenden Arztes, Dr. Schiffmann aufmerksam gemacht.
Dr. Renz Polster hat dazu eine detaillierte und fundierte Replik in seinem Blog ‚Kinder verstehen‘ verfasst. Den Link hierzu füge ich hier gerne an.
https://www.kinder-verstehen.de/mein-werk/blog/corona-so-funktioniert-der-schwindel/?#=
